肿瘤相关超级增强子的研究方案及其在细胞技术研发中的应用前景
引言
超级增强子是基因组上一类由多个相邻的典型增强子簇集而成的、具有超强转录激活能力的顺式调控元件。近年来的研究发现,超级增强子在维持细胞身份、调控发育过程以及驱动多种疾病,尤其是肿瘤的发生发展中起着关键作用。肿瘤相关超级增强子(Tumor-Associated Super-Enhancers, TASEs)的异常激活或形成,是驱动癌基因高表达、促进肿瘤细胞增殖、侵袭和转移的重要机制。因此,深入解析TASEs,不仅有助于揭示肿瘤发生的新机制,也为基于细胞技术的肿瘤诊断和治疗策略研发提供了极具潜力的新靶点和新方向。
一、肿瘤相关超级增强子的核心研究方案
针对TASEs的系统性研究,通常遵循一套多层次、多技术整合的方案。
- 鉴定与图谱绘制:
- 技术手段:主要利用染色质免疫沉淀测序(ChIP-seq),针对组蛋白修饰标记(如H3K27ac)、转录因子(如MED1、BRD4)以及染色质可及性测序(ATAC-seq)等技术,在全基因组范围内鉴定和绘制不同肿瘤类型及细胞系中的超级增强子图谱。
- 分析重点:通过生物信息学分析,比较肿瘤组织与正常组织、不同亚型肿瘤、或治疗前后样本中超级增强子的差异,锁定与肿瘤发生发展特异性相关的TASEs。
- 功能验证与机制解析:
- 基因编辑技术:利用CRISPR/Cas9系统对候选TASEs进行定点删除(deletion)或干扰(干扰其结合蛋白,如使用dCas9-KRAB进行抑制),随后通过RNA-seq、细胞增殖、凋亡、侵袭迁移等实验,在细胞和动物模型中验证其对下游靶基因表达及肿瘤表型的调控功能。
- 染色质构象分析:采用染色质构象捕获技术(如Hi-C、ChIA-PET)揭示TASEs与其靶基因启动子之间的三维空间互作,确认其直接的调控关系。
- 关键因子挖掘:通过质谱分析、蛋白质相互作用研究等手段,鉴定驱动和维持特定TASEs活性的关键转录因子、辅因子和表观遗传阅读器。
- 临床关联与转化研究:
- 分析TASEs的活性或靶基因表达水平与患者临床病理特征(分期、分级、预后)的相关性,评估其作为生物标志物的潜力。
- 探索靶向TASEs或其关键组分的小分子抑制剂(如BET抑制剂、CDK7/9抑制剂)在临床前模型中的疗效,为药物研发提供依据。
二、在细胞技术研发与应用中的广阔前景
对TASEs的深入理解,正直接推动着肿瘤领域细胞技术的革新。
- 新型细胞模型构建:
- 利用对TASEs的操控,可以在正常细胞中“安装”特定的致癌TASEs,或在肿瘤细胞中“关闭”关键TASEs,从而构建出能更精准模拟肿瘤发生、演进或去分化/再分化过程的体外细胞模型。这些模型对于药物筛选和机制研究具有更高保真度。
- 细胞治疗策略的优化:
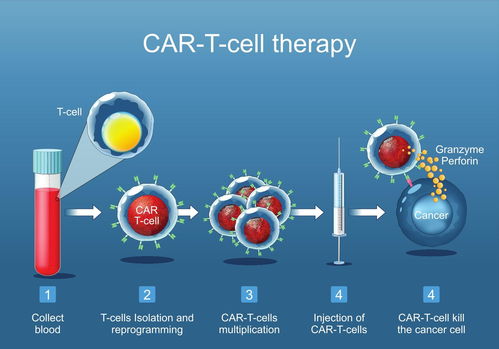
- CAR-T/TCR-T细胞疗法:TASEs研究有助于发现仅在肿瘤细胞中高表达、且对肿瘤存活至关重要的新抗原(由TASEs驱动的基因编码)。这些抗原是设计下一代高特异性、低脱靶毒性CAR-T或TCR-T细胞的理想靶点。
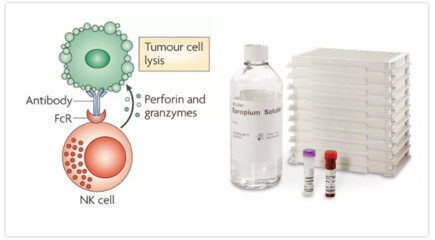
- 免疫细胞功能增强:研究免疫细胞(如T细胞、NK细胞)自身的超级增强子网络,可以通过基因编辑或表观遗传药物定向增强其抗癌相关基因(如细胞因子、效应分子)的表达,从而打造“超级免疫细胞”,提高过继性细胞治疗的持久性和效力。
- 基于细胞的精准诊断与预后判断:
- 从患者体液(如血液、胸腔积液)中分离的循环肿瘤细胞(CTCs)或外泌体中,检测特定TASEs的活性标志,可作为一种微创的“液体活检”手段,用于肿瘤的早期诊断、分子分型、微小残留病灶监测及疗效动态评估。
- 细胞重编程与再生医学中的风险控制:
- 在诱导多能干细胞(iPSC)技术或直接细胞转分化中,对重编程过程中异常激活的、可能致癌的超级增强子进行监测和干预,有助于提高生成细胞的安全性,降低成瘤风险,推动其向临床安全转化。
结论与展望
肿瘤相关超级增强子研究,架起了基础肿瘤生物学与前沿细胞技术应用之间的桥梁。通过系统性的研究方案,我们正不断揭示TASEs在肿瘤中的奥秘。而其应用前景,已深度渗透到从疾病模型构建、新型细胞疗法开发、到精准诊断的整个链条。随着单细胞多组学技术、高分辨率空间转录组学以及更高效的基因编辑工具的进步,对TASEs的动态调控和细胞异质性作用的理解将更加深入。在此基础上,发展出特异性靶向致病TASEs而不过度干扰正常细胞基因组的“表观遗传精准医疗”策略,以及与细胞技术深度融合的个体化治疗方案,将成为战胜肿瘤的重要新武器。
如若转载,请注明出处:http://www.nicellsmall.com/product/24.html
更新时间:2026-05-18 03:00:24