从盘中餐到体内药 细胞培养技术的跨界融合与未来展望
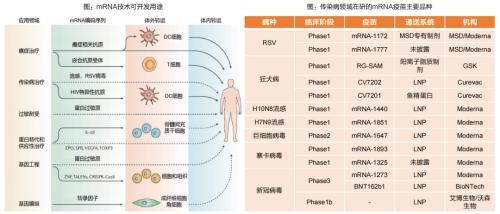
细胞培养技术正以前所未有的速度渗透到多个领域,其中最引人瞩目的莫过于细胞培养肉与细胞疗法。尽管两者在最终应用上看似风马牛不相及——一个旨在重塑我们的食物系统,另一个则致力于攻克人类顽疾——但其底层技术逻辑却有着惊人的同源性。业内人士普遍认为,这种“研发方向不同,但基础原理类似”的现状,正预示着细胞技术一个充满无限可能的未来。
一、 殊途同归:共享的核心技术基石
无论是培育一块可供食用的“细胞肉”,还是制备用于治疗的“活体药物”,其起点都是一样的:细胞。两者都依赖于以下核心技术的支撑:
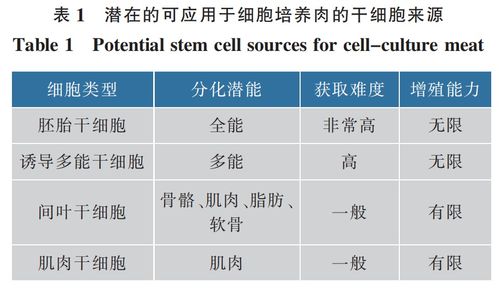
- 细胞系建立与筛选:都需要获取并培养特定的起始细胞(如动物肌肉干细胞或人体免疫细胞、干细胞),并确保其稳定增殖、保持功能。
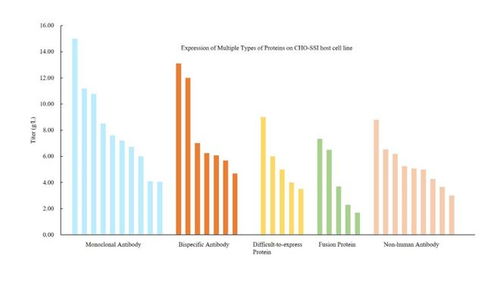
- 细胞培养基与生物反应器:都需要在体外为细胞提供精准的营养、生长因子和物理化学环境(如温度、pH、溶氧),以支持其大规模扩增。生物反应器技术是关键共性平台。
- 组织工程与支架材料:对于细胞肉,需要利用可食用的支架引导肌肉纤维形成三维肉质结构;对于细胞疗法(如组织修复),则需要生物相容性支架构建功能组织。材料科学是交叉点。
- 过程监控与质量控制:都需要严格的无菌操作、实时监测细胞状态,并确保最终产物的安全性、一致性及有效性。
正是这些共享的技术模块,使得两个领域的研发经验、设备平台乃至人才知识能够产生流动与借鉴。
二、 分道扬镳:差异化的研发路径与挑战
尽管起点相似,但不同的终极目标使两者走上了截然不同的研发道路,面临各自的“悬崖”。
- 细胞培养肉:核心目标是 “降本、量产、仿形” 。挑战在于如何将成本降低到与传统肉类竞争的水平;如何将实验室的克级产量提升至工厂的吨级规模;以及如何完美复刻真实肉类的口感、风味和质地。其研发更侧重于工程化放大、食品科学和消费者接受度。
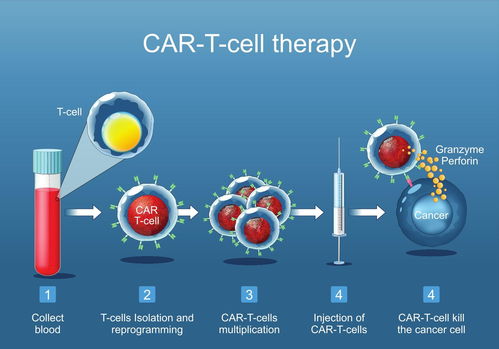
- 细胞疗法:核心目标是 “精准、有效、安全” 。挑战在于确保细胞产品的治疗特异性(如CAR-T细胞精准识别癌细胞)、持久疗效,以及克服潜在的免疫排斥、细胞因子风暴等严重副作用。其研发更侧重于分子生物学、免疫学深度探索和严格的临床医学验证。
可以说,细胞肉研发是一场面向大众市场的“成本与规模”的攻坚战,而细胞疗法则是一场面向个体患者的“精准与安全”的科技前沿赛。
三、 跨界赋能:双向驱动的创新生态
这种“基础同源、应用分流”的格局,并非彼此孤立,反而催生了强大的协同创新效应。
- 从细胞疗法到细胞肉:细胞疗法数十年积累的深层细胞生物学知识、精细的细胞操控技术(如基因编辑)、以及高端生物工艺,为细胞肉在细胞选育、培养效率提升方面提供了高起点。例如,对干细胞自我更新和分化的理解直接助力肌肉干细胞的培养。
- 从细胞肉到细胞疗法:细胞肉产业对大规模、低成本生物制造技术的极致追求,正在倒逼生物反应器设计、培养基配方(寻求无血清、化学成分明确替代方案)、自动化生产流程的革新。这些工程学上的突破,有望显著降低某些细胞疗法高昂的生产成本,使其更可及。
在监管科学、伦理讨论和社会接受度培育方面,两个领域的实践也能相互参照,共同推动建立适应新兴生物技术的治理框架。
四、 未来展望:汇聚于“细胞经济”的蓝海
长远来看,细胞培养肉与细胞疗法代表了“细胞作为生产单元”这一范式的两大应用出口。它们共同隶属于一个更大的愿景——“细胞经济” 。在这个蓝图下,细胞不仅是生命的基础,更是可持续食物、新型材料、再生医学和个性化治疗的先进“生物工厂”。
随着底层技术(如合成生物学、人工智能辅助的细胞设计、新型生物材料)的不断突破,今天在各自赛道攻坚的许多技术成果,明天可能成为另一个赛道的标准配置。未来的生物技术公司,或许将同时布局健康与消费领域,实现技术价值的最大化。
从喂养人类到治愈人类,细胞培养技术正沿着两条清晰而又交织的轨迹飞速发展。它们因共同的基础科学而诞生,因不同的使命而深耕,又终将在推动人类社会向更健康、更可持续未来迈进的道路上,殊途同归。这场始于实验室的细胞革命,其边界正不断拓展,其融合产生的能量,远超我们当前的想象。
如若转载,请注明出处:http://www.nicellsmall.com/product/27.html
更新时间:2026-05-28 06:03:57